Wasserdampfdiffusion im Boden
Storyboard 
Wenn die Konzentration nicht gleichmäßig ist, beginnen Diffusionsprozesse, bei denen sich der Wasserdampf aus Bereichen größerer oder geringerer Konzentration bewegt.
ID:(376, 0)
Wasserdampfdiffusion im Boden
Storyboard 
Wenn die Konzentration nicht gleichmäßig ist, beginnen Diffusionsprozesse, bei denen sich der Wasserdampf aus Bereichen größerer oder geringerer Konzentration bewegt.
Variablen
Berechnungen
Berechnungen
Gleichungen
Der Anzahl der Mol ($n$) entspricht der Anzahl der Partikel ($N$) geteilt durch der Avogadros Nummer ($N_A$):
Wenn wir sowohl den Z hler als auch den Nenner mit die Partikelmasse ($m$) multiplizieren, erhalten wir:
$n=\displaystyle\frac{N}{N_A}=\displaystyle\frac{Nm}{N_Am}=\displaystyle\frac{M}{M_m}$
Also ist es:
Mit die Partikelkonzentration ($c_n$) als der Anzahl der Partikel ($N$) und der Volumen ($V$) erhalten wir:
Mit die Partikelmasse ($m$) und die Masse ($M$),
Da die Dichte ($\rho$) ist
erhalten wir
$c_n=\displaystyle\frac{N}{V}=\displaystyle\frac{M}{mV}=\displaystyle\frac{\rho}{m}$
Deshalb,
Beispiele
Wenn sich ein Teilchen eines Gases bewegt, interagiert es mit anderen Teilchen. Die einfachste Form dieser Interaktion erfolgt durch elastische St e, was bedeutet, dass das Teilchen ohne Energieverlust kollidiert und seine Richtung ndert, um ein anderes Teilchen zu treffen.
Im Rahmen dieses Prozesses macht es Sinn, der Freier Weg ($\bar{l}$) zu definieren, dessen Wert von ERROR:5548.1 abh ngen wird.
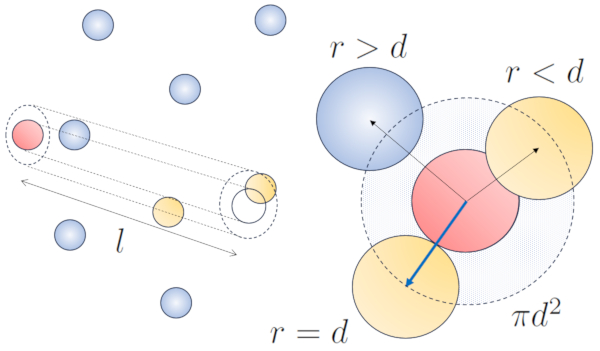
Wenn ein Teilchen mit einem gegebenen Radius sich im Raum bewegt, nimmt es effektiv den Raum eines Zylinders mit dem gleichen Radius ein. Damit ein Teilchen mit einem anderen kollidiert, muss sich dieses zweite Teilchen teilweise innerhalb dieses Zylinders befinden. Im extremsten Fall befindet sich das zweite Teilchen in einem Abstand von zwei Radien vom ersten Teilchen, so dass die Kante des Zylinders einen Punkt auf der Kugel ber hrt, der dem Zylinderachsen am n chsten liegt. Das Zentrum dieser Kugel ist einen Radius entfernt von der Oberfl che des Zylinders:
Daher betr gt der Abstand zwischen der Achse des Zylinders und dem Zentrum eines beliebigen Teilchens zwei Radien, oder anders ausgedr ckt, ein Durchmesser. Im Wesentlichen kann man sich vorstellen, dass das tats chlich vom sich durch den Raum bewegenden Teilchen eingenommene Volumen einem Zylinder mit einer L nge entspricht, die dem freien Weg entspricht, und einem Radius, der dem Durchmesser des Teilchens entspricht.
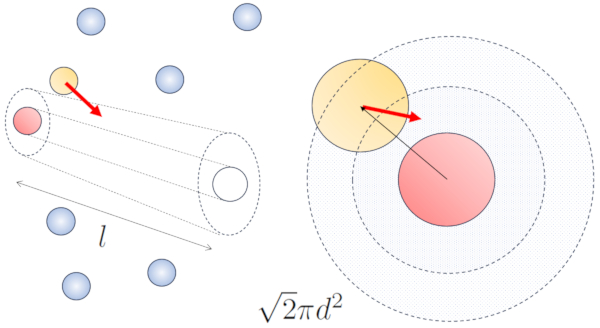
Wenn benachbarte Teilchen sich bewegen, besteht eine h here Wahrscheinlichkeit f r Kollisionen, da sie in derselben Zeitspanne eine gr ere Strecke zur cklegen. Die Geschwindigkeitskomponenten $v_x$, $v_y$ und $v_z$ schwanken um Mittelwerte von $\sqrt{\langle v_x^2\rangle}$, $\sqrt{\langle v_y^2\rangle}$ und $\sqrt{\langle v_z^2\rangle}$. Unter der Annahme, dass das System isotrop ist, wird der Durchschnitt jeder Komponente gleich $\displaystyle\frac{1}{3}\sqrt{\langle v^2\rangle}$ sein. Daher wird entlang der Achse, entlang der die Partikel sich bewegen, eine Strecke zur ckgelegt
$\sqrt{\langle v_z^2\rangle}dt=\displaystyle\frac{1}{3}\sqrt{\langle v^2\rangle}dt$
Zur gleichen Zeit haben Teilchen, die sich senkrecht bewegen, eine Strecke zur ckgelegt:
$\sqrt{\langle v_x^2\rangle+\langle v_y^2\rangle}dt=\displaystyle\frac{\sqrt{2}}{3}\sqrt{\langle v^2\rangle}dt$
Daher erh ht sich die Wahrscheinlichkeit einer Kollision um den Faktor $\sqrt{2}$ im Vergleich zum Fall, in dem sich die Partikel nicht bewegen:
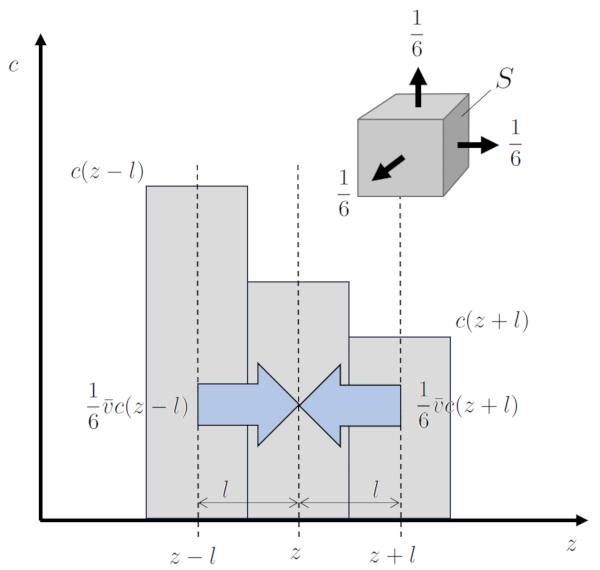
Wenn es einen r umlichen Unterschied in die Partikelkonzentration ($c_n$) gibt, tritt ein Ph nomen auf, das als ERROR:6597,0 bekannt ist. Die Wahrscheinlichkeit, dass Teilchen von einer Position vor einer Entfernung von der Freier Weg ($\bar{l}$) zu eine Positionieren Sie entlang einer Achse ($z$) gelangen, unterscheidet sich von der Wahrscheinlichkeit von einer Position nach derselben Entfernung. Dies f hrt zu Ver nderungen in die Partikelkonzentration ($c_n$), einem Prozess, der als Diffusion bekannt ist. Die Geschwindigkeit, mit der dieser Prozess stattfindet, ist die von die Durchschnittsgeschwindigkeit eines Teilchens ($\bar{v}$), und daran beteiligen sich jeweils $1/6$ der Partikel in jede Richtung, da es insgesamt 6 Richtungen in einem dreidimensionalen Raum gibt.
Auf diese Weise wird die Teilchenflussdichte ($j$) generiert, das in Bezug auf die Fl che folgenderma en entspricht:
$j=\displaystyle\frac{1}{6}\bar{v}c(z-\bar{l}) - \displaystyle\frac{1}{6}\bar{v}c(z+\bar{l})=\displaystyle\frac{1}{6}\bar{v}[c(z-\bar{l})-c(z+\bar{l})]=-\displaystyle\frac{1}{6}\bar{v}2\bar{l}\displaystyle\frac{dc}{dz}$
Die Konstanten, die beim Berechnen von die Teilchenflussdichte ($j$) faktorisiert werden, werden in einer Konstanten zusammengefasst, die als die Diffusionskonstante ($D$) bezeichnet wird und gleich einem Drittel des Produkts von der Freier Weg ($\bar{l}$) und die Durchschnittsgeschwindigkeit eines Teilchens ($\bar{v}$) ist.
Die Berechnung von die Teilchenflussdichte ($j$) basierend auf die Konzentrationsvariation ($dc_n$), ERROR:10192,0 und die Diffusionskonstante ($D$):
erm glicht es uns, zu bestimmen, wie Wasser aus dem Grundwasserspiegel verdunstet. Dazu sind folgende Schritte erforderlich:
• Die Umgebungstemperatur, relative Luftfeuchtigkeit, Bodenporosit t und die Tiefe des Grundwasserspiegels ermitteln.
• Die Wassertemperatur an der Oberfl che des Grundwasserspiegels berechnen.
• Die ges ttigte Wasserdampfkonzentration ber dem Grundwasserspiegel berechnen.
• Die Wasserdampfkonzentration ber dem Boden berechnen.
• Den Wasserdampffluss f r die station re Flie grenze berechnen.
Die Molare Konzentration ($c_m$) entspricht ERROR:9339,0 geteilt durch der Volumen ($V$) eines Gases und wird wie folgt berechnet:
Der Anzahl der Mol ($n$) entspricht der Anzahl der Partikel ($N$) geteilt durch der Avogadros Nummer ($N_A$):
der Avogadros Nummer ($N_A$) ist eine universelle Konstante mit dem Wert 6.028E+23 1/mol und wird daher nicht zu den im Rechenprozess verwendeten Variablen gez hlt.
Um die Molare Konzentration ($c_m$) in die Partikelkonzentration ($c_n$) umzuwandeln, multiplizieren Sie einfach die erste Zahl mit der Avogadros Nummer ($N_A$), wie folgt:
Der Anzahl der Mol ($n$) wird ermittelt, indem man die Masse ($M$) einer Substanz durch ihr die Molmasse ($M_m$) teilt, was dem Gewicht eines Mols der Substanz entspricht.
Daher kann die folgende Beziehung hergestellt werden:
Die molare Masse wird in Gramm pro Mol (g/mol) ausgedr ckt.
Wenn wir die Dichte ($\rho$) durch die Partikelmasse ($m$) teilen, erhalten wir die Partikelkonzentration ($c_n$):
Der mittlere freie Weg kann in Abh ngigkeit vom Durchmesser eines imagin ren Zylinders gesch tzt werden, der eine Partikel umgibt und im Durchschnitt eine Kollision mit einer anderen Partikel hat.
Der Radius des Zylinders entspricht dem maximalen Abstand, den zwei Partikel haben m ssen, um zu kollidieren, was dem doppelten Radius der Partikel entspricht, d.h. Der Partikeldurchmesser ($d$). Da innerhalb dieses Zylinders nur eine Kollision stattfindet, muss die Anzahl der darin enthaltenen Partikel gleich eins sein. Das bedeutet:
$l d^2\pi c_n= 1$
mit die Partikelkonzentration ($c_n$), und wenn wir nach der Freier Weg ($\bar{l}$) aufl sen, erhalten wir:
Dies stellt den mittleren freien Weg dar.
F r den Fall ohne Bewegung betr gt die Wahrscheinlichkeit der Freier Weg ($\bar{l}$), w hrend sie sich bei Bewegung auf der Partikeldurchmesser ($d$) und die Partikelkonzentration ($c_n$) ndert.
Im Fall der Bewegung steigt die Wahrscheinlichkeit um den Faktor $\sqrt{2}$, was bedeutet, dass der freie Weg betr gt
Die Kinetische Energie ($K$) in Kombination mit die Partikelmasse ($m$) und die Durchschnittsgeschwindigkeit eines Teilchens ($\bar{v}$) ergibt
Hinweis: In strengerem Sinne h ngt die kinetische Energie vom Durchschnitt der Geschwindigkeit zum Quadrat $\bar{v^2}$ ab. Es wird jedoch angenommen, dass dies ungef hr gleich dem Quadrat des Durchschnitts der Geschwindigkeit ist:
$\bar{v^2}\sim\bar{v}^2$
Die Partikelmasse ($m$) kann aus die Molmasse ($M_m$) und der Avogadros Nummer ($N_A$) gesch tzt werden mithilfe von
Das Stefan-Boltzmann-Gesetz, das urspr nglich von Josef Stefan [1] formuliert und sp ter von Ludwig Boltzmann [2] weiterentwickelt wurde, besagt, dass die Energie eines Moleküls ($E$) proportional zu das Freiheitsgrade ($f$) multipliziert mit die Absolute Temperatur ($T$) ist, wobei eine Proportionalit tskonstante von die Boltzmann-Konstante ($k_B$) vorliegt:
Es ist wichtig zu beachten, dass die Absolute Temperatur ($T$) unbedingt in Kelvin ausgedr ckt werden muss.
Die Anzahl der Freiheitsgrade eines Teilchens entspricht der Anzahl der Variablen, die erforderlich sind, um seinen thermodynamischen Zustand zu beschreiben. Zum Beispiel ben tigt ein Punktteilchen nur drei Koordinaten, was zu drei Freiheitsgraden f hrt. Wenn das Teilchen jedoch eine Form und Steifigkeit aufweist, sind zwei zus tzliche Winkel erforderlich, was zu insgesamt f nf Freiheitsgraden f hrt. Wenn das Teilchen sich zus tzlich deformieren oder in einer oder mehreren Richtungen schwingen kann, werden diese zus tzlichen Modi ebenfalls als zus tzliche Freiheitsgrade betrachtet. Es ist jedoch wichtig zu beachten, dass diese zus tzlichen Freiheitsgrade nur bei hohen Temperaturen existieren, wenn das Teilchen gen gend Energie hat, um solche Schwingungen zu aktivieren.
[1] " ber die Beziehung zwischen der W rmestrahlung und der Temperatur" ( ber die Beziehung zwischen der W rmestrahlung und der Temperatur), Josef Stefan, Sitzungsberichte der mathematisch-naturwissenschaftlichen Classe der Kaiserlichen Akademie der Wissenschaften, Wien (1879).
[2] "Weitere Studien ber das W rmegleichgewicht unter Gasmolek len" (Weitere Studien ber das W rmegleichgewicht unter Gasmolek len), Ludwig Boltzmann, Sitzungsberichte der mathematisch-naturwissenschaftlichen Classe der Kaiserlichen Akademie der Wissenschaften, Wien (1884).
Como la energ a cin tica de la mol cula es
y la energ a en funci n de la temperatura es
con
Die Diffusionskonstante $D$ kann aus der durchschnittlichen Geschwindigkeit $\bar{v}$ und dem mittleren freien Weg $\bar{l}$ der Teilchen berechnet werden.
Es ist wichtig zu erkennen, dass sowohl der mittlere freie Weg als auch die Durchschnittsgeschwindigkeit von der Temperatur abh ngen, und folglich auch die Diffusionskonstante. Daher wird bei der Ver ffentlichung von Werten f r die sogenannte Konstante immer die Temperatur angegeben, auf die sie sich bezieht.
Im Jahr 1855 formulierte Adolf Fick [1] eine Gleichung zur Berechnung von die Diffusionskonstante ($D$), was zu die Teilchenflussdichte ($j$) aufgrund von die Konzentrationsvariation ($dc_n$) entlang ERROR:10192,0 f hrt:
[1] " ber Diffusion", Adolf Fick, Annalen der Physik und Chemie, Band 170, Seiten 59-86 (1855)
In einer Dimension wird die Teilchenflussdichte ($j$) unter Verwendung der Werte die Diffusionskonstante ($D$), die Partikelkonzentration ($c_n$) und die Positionieren Sie entlang einer Achse ($z$) gem dem Fickschen Gesetz [1] berechnet:
Diese Formel kann f r mehr als eine Dimension verallgemeinert werden wie folgt:
[1] " ber Diffusion", Adolf Fick, Annalen der Physik und Chemie, Band 170, Seiten 59-86 (1855)
Wenn die Diffusionskonstante ($D$) gleich die Teilchenflussdichte ($j$) ist aufgrund von die Konzentrationsvariation ($dc_n$) entlang ERROR:10192,0, wird dies durch das Gesetz von Fick [1] geregelt:
Daher erhalten wir zur Beschreibung der Konzentrations nderung bei der Zeit ($t$), die der r umlichen nderung der Flussdichte entspricht, die Gleichung
[1] " ber Diffusion" ( ber Diffusion), Adolf Fick, Annalen der Physik und Chemie, Band 170, Seiten 59-86 (1855).
ID:(376, 0)