Calor y Temperatura
Storyboard 
El calor es la energía contenida en los átomos de un cuerpo, manifestándose como oscilaciones alrededor de su posición de equilibrio.La temperatura es una indicación de esta energía térmica. Al añadir calor a un objeto, su temperatura aumenta de manera proporcional. La constante de esta proporcionalidad se llama capacidad calórica, que es, de hecho, una función dependiente de la temperatura.
ID:(780, 0)
Mecanismos
Concepto 
El calor y la temperatura son conceptos fundamentales en la termodinámica que representan diferentes cantidades físicas. El calor es la energía transferida entre sistemas u objetos debido a una diferencia de temperatura, fluyendo de objetos más calientes a más fríos hasta que se alcanza el equilibrio térmico. Se mide en joules, calorías o unidades térmicas británicas y se considera una función de trayectoria, lo que significa que depende del proceso de transferencia de energía. El calor puede transferirse a través de conducción, convección o radiación.
La temperatura, por otro lado, es una medida de la energía cinética promedio de las partículas en una sustancia, indicando qué tan caliente o frío está un objeto. Se mide en grados Celsius, Kelvin o Fahrenheit, siendo el Kelvin la unidad del SI utilizada en contextos científicos. La temperatura es una función de estado, dependiendo solo del estado actual del sistema y no del proceso utilizado para alcanzar ese estado. Determina la dirección del flujo de calor, ya que el calor se mueve de regiones de mayor temperatura a regiones de menor temperatura.
ID:(15242, 0)
Calor microscópico
Descripción 
El calor no es más que energía a nivel microscópico.
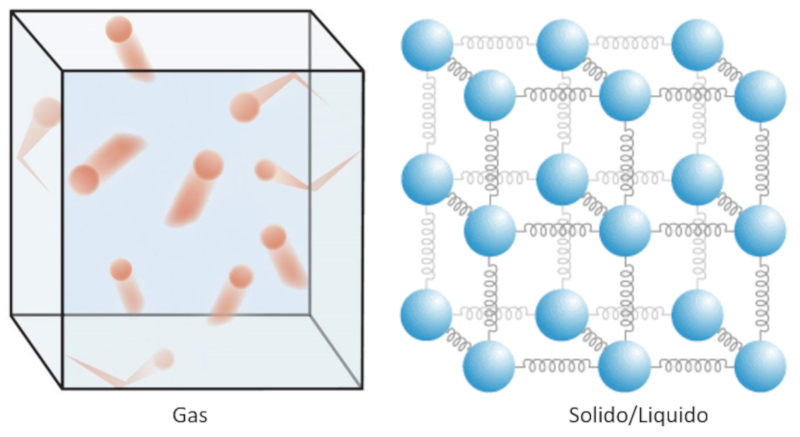
En el caso de un gas, se relaciona principalmente con la energía cinética de sus moléculas.En líquidos y sólidos, debemos tener en cuenta la atracción entre los átomos, por lo que la energía potencial también desempeña un papel importante. En este caso, el calor corresponde a la energía que poseen las partículas y con la cual oscilan alrededor del punto de equilibrio definido por las demás partículas en su entorno.
ID:(118, 0)
Calor
Descripción 
El calor está estrechamente relacionado con elementos como el fuego, que eleva la temperatura del agua. El proceso de calentamiento genera movimiento, lo cual demuestra que el calor está asociado con la energía mecánica. Incluso el mango de una olla se calienta, y nuestro cuerpo es capaz de percibir esa temperatura. Además, el fuego emite radiación, la cual calienta los objetos que son irradiados.
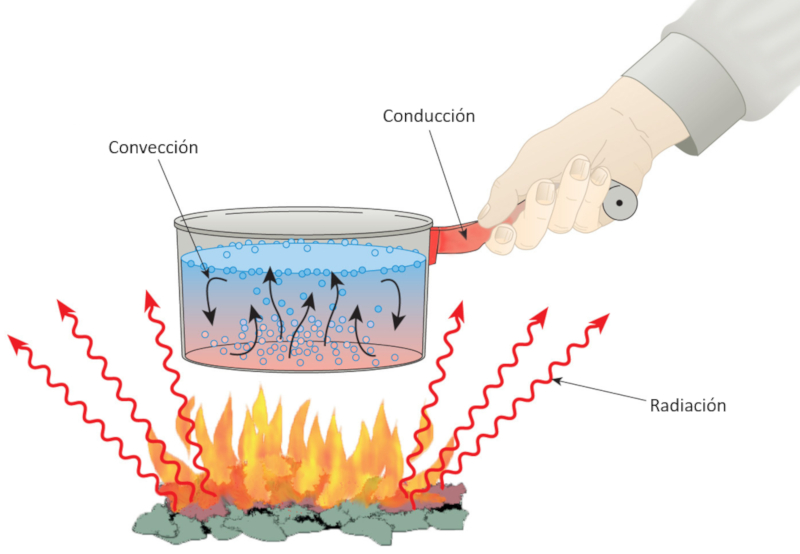
Podemos inferir, por lo tanto, que al transferir calor a un objeto, podemos aumentar su temperatura, y que la generación de movimiento está asociada con la energía.
ID:(585, 0)
Temperatura
Descripción 
La temperatura es una medida de la energía contenida en un cuerpo y está asociada, en sólidos y líquidos, a las oscilaciones de las moléculas o átomos, y en gases y líquidos, al desplazamiento de estas partículas.

ID:(11118, 0)
Calor y Temperatura
Modelo 
El calor es la energía contenida en los átomos de un cuerpo, manifestándose como oscilaciones alrededor de su posición de equilibrio. La temperatura es una indicación de esta energía térmica. Al añadir calor a un objeto, su temperatura aumenta de manera proporcional. La constante de esta proporcionalidad se llama capacidad calórica, que es, de hecho, una función dependiente de la temperatura.
Variables
Cálculos
Cálculos
Ecuaciones
(ID 3197)
(ID 4381)
(ID 12772)
Ejemplos
El calor y la temperatura son conceptos fundamentales en la termodin mica que representan diferentes cantidades f sicas. El calor es la energ a transferida entre sistemas u objetos debido a una diferencia de temperatura, fluyendo de objetos m s calientes a m s fr os hasta que se alcanza el equilibrio t rmico. Se mide en joules, calor as o unidades t rmicas brit nicas y se considera una funci n de trayectoria, lo que significa que depende del proceso de transferencia de energ a. El calor puede transferirse a trav s de conducci n, convecci n o radiaci n.
La temperatura, por otro lado, es una medida de la energ a cin tica promedio de las part culas en una sustancia, indicando qu tan caliente o fr o est un objeto. Se mide en grados Celsius, Kelvin o Fahrenheit, siendo el Kelvin la unidad del SI utilizada en contextos cient ficos. La temperatura es una funci n de estado, dependiendo solo del estado actual del sistema y no del proceso utilizado para alcanzar ese estado. Determina la direcci n del flujo de calor, ya que el calor se mueve de regiones de mayor temperatura a regiones de menor temperatura.
(ID 15242)
El calor no es m s que energ a a nivel microsc pico.

En el caso de un gas, se relaciona principalmente con la energ a cin tica de sus mol culas.En l quidos y s lidos, debemos tener en cuenta la atracci n entre los tomos, por lo que la energ a potencial tambi n desempe a un papel importante. En este caso, el calor corresponde a la energ a que poseen las part culas y con la cual oscilan alrededor del punto de equilibrio definido por las dem s part culas en su entorno.
(ID 118)
El calor est estrechamente relacionado con elementos como el fuego, que eleva la temperatura del agua. El proceso de calentamiento genera movimiento, lo cual demuestra que el calor est asociado con la energ a mec nica. Incluso el mango de una olla se calienta, y nuestro cuerpo es capaz de percibir esa temperatura. Adem s, el fuego emite radiaci n, la cual calienta los objetos que son irradiados.

Podemos inferir, por lo tanto, que al transferir calor a un objeto, podemos aumentar su temperatura, y que la generaci n de movimiento est asociada con la energ a.
(ID 585)
La temperatura es una medida de la energ a contenida en un cuerpo y est asociada, en s lidos y l quidos, a las oscilaciones de las mol culas o tomos, y en gases y l quidos, al desplazamiento de estas part culas.

(ID 11118)
(ID 15243)
ID:(780, 0)
