Tercera Ley de la Termodinámica
Storyboard 
La tercera ley de la termodinámica establece que, al acercarse al límite de temperatura absoluta cero, la entropía de un sistema alcanza un valor constante. Generalmente, esta constante es cero, lo que implica que existe un único estado microscópico posible para el sistema.
ID:(1468, 0)
Mecanismos
Definición 
La tercera ley de la termodinámica establece que a medida que un sistema se aproxima al cero absoluto, la entropía del sistema se aproxima a un valor mínimo. En el cero absoluto, la entropía de una sustancia perfectamente cristalina se vuelve cero. Esta ley implica que es imposible alcanzar el cero absoluto mediante un número finito de procesos. La tercera ley también proporciona un punto de referencia para la determinación de la entropía, asegurando que los valores de entropía sean absolutos y no relativos. Tiene implicaciones significativas para el comportamiento de los materiales a temperaturas muy bajas, influyendo en fenómenos como la superconductividad y el calor específico de las sustancias. En esencia, la tercera ley establece una base para la entropía y destaca la inalcanzabilidad del cero absoluto, enfatizando las limitaciones inherentes en los procesos de enfriamiento.
ID:(15252, 0)
Tercera ley de la termodinámica
Imagen 
La tercera ley de la termodinámica [1] establece que a medida que la la temperatura absoluta ($T$) de un sistema se aproxima al cero absoluto, la la entropía en el limite temperatura nula ($S$) de una sustancia cristalina perfecta se aproxima a un valor mínimo, típicamente cero. Esto implica que es imposible alcanzar el cero absoluto a través de un número finito de procesos porque la entropía se volvería constante. Esencialmente, la tercera ley establece que la entropía de un cristal perfecto en el cero absoluto es cero y destaca la inalcanzabilidad del cero absoluto debido a la cantidad infinita de energía necesaria para su eliminación.
| $\lim_{T\rightarrow 0}S=0$ |
Esta ley tiene implicaciones significativas para comprender el comportamiento de los materiales a temperaturas muy bajas y proporciona un punto de referencia fundamental para calcular los valores de entropía.
![]() [1] "Über die Berechnung chemischer Gleichgewichte aus thermischen Messungen" (Sobre el cálculo de los equilibrios químicos a partir de mediciones térmicas), Walther Nernst, Nachrichten von der Gesellschaft der Wissenschaften zu Göttingen, Mathematisch-Physikalische Klasse, 1906
[1] "Über die Berechnung chemischer Gleichgewichte aus thermischen Messungen" (Sobre el cálculo de los equilibrios químicos a partir de mediciones térmicas), Walther Nernst, Nachrichten von der Gesellschaft der Wissenschaften zu Göttingen, Mathematisch-Physikalische Klasse, 1906
ID:(11130, 0)
Calculo de la entropía
Nota 
La relación de la variación de calor ($\delta Q$) con la temperatura absoluta ($T$) y la variación de la entropía ($dS$) se puede expresar de la siguiente manera:
| $ \delta Q = T dS $ |
Cuando combinamos esto con la relación entre la calor suministrado al liquido o solido ($\Delta Q$), la capacidad Calórica ($C$) y la variación de la temperatura ($\Delta T$):
| $ \delta Q = C dT $ |
Obtenemos esta relación en el límite infinitesimal, donde:
$\delta Q = C dT = T dS$
Después de la integración, llegamos a la siguiente ecuación:
| $ S = S_0 + C \log\left(\displaystyle\frac{ T }{ T_0 }\right)$ |
con la condición de que la entropía base ($S_0$) sea menor que la temperatura base ($T_0$).
ID:(15705, 0)
Entropía y cambio de Fase
Cita 
Si se estima la entropía en función de la temperatura, se observará lo siguiente:
• En cada fase (sólido, líquido, gas), la entropía tiende a aumentar ligeramente con la temperatura.
• En cada cambio de fase, experimenta un salto.
Esto se puede representar de la siguiente manera:
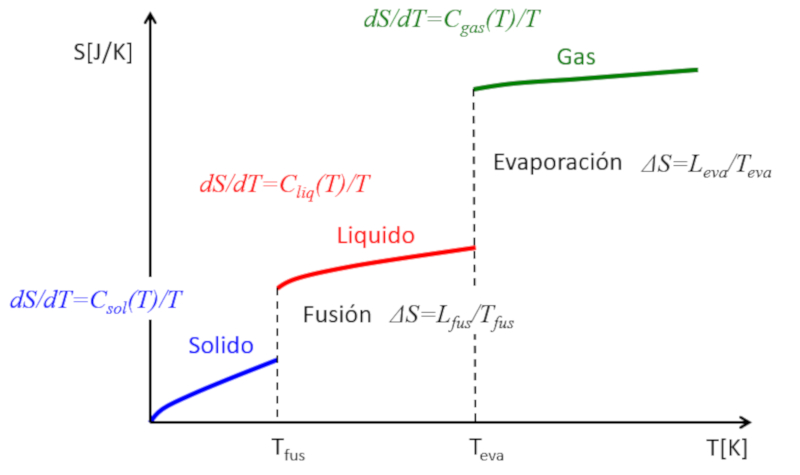
De esta forma, se puede entender la entropía como una medida de los grados de libertad que tiene un sistema. Mientras que en una fase la entropía aumenta gradualmente debido a la liberación de pocos grados de libertad adicionales, en los cambios de fase el incremento es drástico. Un sólido está compuesto por múltiples enlaces que impiden el movimiento de los átomos. En un líquido, se pierden muchos enlaces, lo que crea nuevas libertades que permiten el desplazamiento relativo, asociado a múltiples nuevos grados de libertad. Finalmente, en la transición al estado gaseoso, se pierden todos los enlaces y cada partícula tiene sus tres grados de libertad. Si se incrementa aún más la temperatura, se observa cómo las partículas pueden rotar e incluso oscilar, lo que representa nuevos grados de libertad y mayores incrementos en la entropía.
ID:(11187, 0)
Tercera Ley de la Termodinámica
Descripción 
La tercera ley de la termodinámica establece que, al acercarse al límite de temperatura absoluta cero, la entropía de un sistema alcanza un valor constante. Generalmente, esta constante es cero, lo que implica que existe un único estado microscópico posible para el sistema.
Variables
Cálculos
Cálculos
Ecuaciones
(ID 3197)
(ID 9639)
(ID 10270)
La relaci n de la variación de calor ($\delta Q$) con la temperatura absoluta ($T$) y la variación de la entropía ($dS$) se puede expresar de la siguiente manera:
| $ \delta Q = T dS $ |
Cuando combinamos esto con la relaci n entre la calor suministrado al liquido o solido ($\Delta Q$), la capacidad Calórica ($C$) y la variación de la temperatura ($\Delta T$):
| $ \delta Q = C dT $ |
Obtenemos esta relaci n en el l mite infinitesimal, donde:
$\delta Q = C dT = T dS$
Despu s de la integraci n, llegamos a la siguiente ecuaci n:
| $ S = S_0 + C \log\left(\displaystyle\frac{ T }{ T_0 }\right)$ |
con la condici n de que la entropía base ($S_0$) sea menor que la temperatura base ($T_0$).
(ID 11185)
Ejemplos
La tercera ley de la termodin mica establece que a medida que un sistema se aproxima al cero absoluto, la entrop a del sistema se aproxima a un valor m nimo. En el cero absoluto, la entrop a de una sustancia perfectamente cristalina se vuelve cero. Esta ley implica que es imposible alcanzar el cero absoluto mediante un n mero finito de procesos. La tercera ley tambi n proporciona un punto de referencia para la determinaci n de la entrop a, asegurando que los valores de entrop a sean absolutos y no relativos. Tiene implicaciones significativas para el comportamiento de los materiales a temperaturas muy bajas, influyendo en fen menos como la superconductividad y el calor espec fico de las sustancias. En esencia, la tercera ley establece una base para la entrop a y destaca la inalcanzabilidad del cero absoluto, enfatizando las limitaciones inherentes en los procesos de enfriamiento.
(ID 15252)
La tercera ley de la termodin mica [1] establece que a medida que la la temperatura absoluta ($T$) de un sistema se aproxima al cero absoluto, la la entropía en el limite temperatura nula ($S$) de una sustancia cristalina perfecta se aproxima a un valor m nimo, t picamente cero. Esto implica que es imposible alcanzar el cero absoluto a trav s de un n mero finito de procesos porque la entrop a se volver a constante. Esencialmente, la tercera ley establece que la entrop a de un cristal perfecto en el cero absoluto es cero y destaca la inalcanzabilidad del cero absoluto debido a la cantidad infinita de energ a necesaria para su eliminaci n.
| $\lim_{T\rightarrow 0}S=0$ |
Esta ley tiene implicaciones significativas para comprender el comportamiento de los materiales a temperaturas muy bajas y proporciona un punto de referencia fundamental para calcular los valores de entrop a.
![]() [1] " ber die Berechnung chemischer Gleichgewichte aus thermischen Messungen" (Sobre el c lculo de los equilibrios qu micos a partir de mediciones t rmicas), Walther Nernst, Nachrichten von der Gesellschaft der Wissenschaften zu G ttingen, Mathematisch-Physikalische Klasse, 1906
[1] " ber die Berechnung chemischer Gleichgewichte aus thermischen Messungen" (Sobre el c lculo de los equilibrios qu micos a partir de mediciones t rmicas), Walther Nernst, Nachrichten von der Gesellschaft der Wissenschaften zu G ttingen, Mathematisch-Physikalische Klasse, 1906
(ID 11130)
La relaci n de la variación de calor ($\delta Q$) con la temperatura absoluta ($T$) y la variación de la entropía ($dS$) se puede expresar de la siguiente manera:
| $ \delta Q = T dS $ |
Cuando combinamos esto con la relaci n entre la calor suministrado al liquido o solido ($\Delta Q$), la capacidad Calórica ($C$) y la variación de la temperatura ($\Delta T$):
| $ \delta Q = C dT $ |
Obtenemos esta relaci n en el l mite infinitesimal, donde:
$\delta Q = C dT = T dS$
Despu s de la integraci n, llegamos a la siguiente ecuaci n:
| $ S = S_0 + C \log\left(\displaystyle\frac{ T }{ T_0 }\right)$ |
con la condici n de que la entropía base ($S_0$) sea menor que la temperatura base ($T_0$).
(ID 15705)
Si se estima la entrop a en funci n de la temperatura, se observar lo siguiente:
• En cada fase (s lido, l quido, gas), la entrop a tiende a aumentar ligeramente con la temperatura.
• En cada cambio de fase, experimenta un salto.
Esto se puede representar de la siguiente manera:

De esta forma, se puede entender la entrop a como una medida de los grados de libertad que tiene un sistema. Mientras que en una fase la entrop a aumenta gradualmente debido a la liberaci n de pocos grados de libertad adicionales, en los cambios de fase el incremento es dr stico. Un s lido est compuesto por m ltiples enlaces que impiden el movimiento de los tomos. En un l quido, se pierden muchos enlaces, lo que crea nuevas libertades que permiten el desplazamiento relativo, asociado a m ltiples nuevos grados de libertad. Finalmente, en la transici n al estado gaseoso, se pierden todos los enlaces y cada part cula tiene sus tres grados de libertad. Si se incrementa a n m s la temperatura, se observa c mo las part culas pueden rotar e incluso oscilar, lo que representa nuevos grados de libertad y mayores incrementos en la entrop a.
(ID 11187)
(ID 15311)
La tercera ley de la termodin mica establece que si un sistema se lleva al cero absoluto, su entrop a se reducir a cero. Esto se puede expresar de la siguiente manera:
| $\lim_{T\rightarrow 0}S=0$ |
(ID 10270)
El diferencial inexacto del calor ($\delta Q$) es igual a la temperatura absoluta ($T$) por la variación de la entropía ($dS$):
| $ \delta Q = T dS $ |
(ID 9639)
Cuando se a aden la calor suministrado al liquido o solido ($\Delta Q$) a un cuerpo, se observa un aumento de la variación de la temperatura ($\Delta T$) de manera proporcional. Por lo tanto, podemos introducir una constante de proporcionalidad la capacidad calórica ($C$), llamada capacidad t rmica, que establece la siguiente relaci n:
| $ \Delta Q = C \Delta T $ |
(ID 3197)
La entropía ($S$) es una funci n de la temperatura absoluta ($T$) con la entropía base ($S_0$) y la temperatura base ($T_0$) seg n:
| $ S = S_0 + C \log\left(\displaystyle\frac{ T }{ T_0 }\right)$ |
(ID 11185)
ID:(1468, 0)
