Aplicación a Gas de Van der Waals
Storyboard 
La ecuación de estado de Van der Waals tiene la peculiaridad de describir estados que no son estables. Un análisis mas detallado muestran que representan la fase liquida del sistema. Su estudio muestra como se puede emplear la energía libre de Gibbs para entender un sistema de dos fases.
Como referencia se puede consultar el articulo Thermodynamic Properties of the van der Waals Fluid de David C. Johnston.
ID:(556, 0)
Gas de Van der Waals y cambio de fase
Definición 
Dado que el mínimo de la energía de Gibbs requiere de que la compresibilidad sea positiva con
| $\left(\displaystyle\frac{\partial^2 G_0}{\partial V^2}\right)_T=-\left(\displaystyle\frac{\partial\bar{p}}{\partial V}\right)_T$ |
se concluye que al ser con
| $ k_p =-\displaystyle\frac{ DV_{p,T} }{ V }$ |
\\n\\nla ecuación de Van der Waals muestra una inestable en la sección en que\\n\\n
$\displaystyle\frac{\partial p}{\partial V}> 0$
La región inestable separa una región de gran volumen molar y de alta compresibilidad, como en un gas, de una región de bajo volumen molar y baja compresibilidad, como en un liquido. Por ello se visualiza que la ecuación de Van der Waals podría representar un gas pero también, en condiciones apropiadas, un liquido. El sector de inestabilidad estaría relacionado con el cambio de fase.
ID:(9044, 0)
Constantes de Van der Waals
Cita 
Las siguientes constantes de la ecuación de Van der Waals:
En Sistema Internacional (SI)
Compuesto | a (J m3/mol2) | b (10-3 m3/mol)
----------------|:------------------:|:---------------------:
Ácido acético | 1.782 | 0.1068
Anhídrido acético | 2.016 | 0.1263
Acetona | 1.409 | 0.0994
Acetonitrilo | 1.781 | 0.1168
Acetileno | 0.445 | 0.05136
Amoníaco | 0.423 | 0.03707
Argón | 0.136 | 0.03219
Benceno | 1.824 | 0.1154
Bromobenceno | 2.894 | 0.1539
Butano | 1.466 | 0.1226
Dióxido de carbono | 0.364 | 0.04267
Sulfuro de carbono | 1.177 | 0.07685
Monóxido de carbono | 0.151 | 0.03985
Cloruro de carbono (IV) | 1.975 | 0.1281
Cloro | 0.658 | 0.05622
Clorobenceno | 2.577 | 0.1453
Cloroetano | 1.105 | 0.08651
Clorometano | 0.757 | 0.06483
Cianógeno | 0.777 | 0.06901
Ciclohexano | 2.311 | 0.1424
Éter dietílico | 1.761 | 0.1344
Sulfuro de dietilo | 1.900 | 0.1214
Éter de dimetilo | 0.818 | 0.07246
Sulfuro de dimetilo | 1.304 | 0.09213
Etano | 0.556 | 0.0638
Etanotiol | 1.139 | 0.08098
Etanol | 1.218 | 0.08407
Acetato de etilo | 2.072 | 0.1412
Etilamina | 1.074 | 0.08409
Fluorobenceno | 2.019 | 0.1286
Fluorometano | 0.469 | 0.05264
Freón | 1.078 | 0.0998
Tetracloruro de germanio | 2.290 | 0.1485
Helio | 0.0035 | 0.0237
Hexano | 2.471 | 0.1735
Hidrógeno | 0.0248 | 0.02661
Bromuro de hidrógeno | 0.4510 | 0.04431
Cloruro de hidrógeno | 0.372 | 0.04081
Seleniuro de hidrógeno | 0.534 | 0.04637
Sulfuro de hidrógeno | 0.449 | 0.04287
Iodobenceno | 3.352 | 0.1656
Kriptón | 0.235 | 0.03978
Mercurio | 0.820 | 0.01696
Metano | 0.228 | 0.04278
Metanol | 0.965 | 0.06702
Neón | 0.0213 | 0.01709
Óxido nítrico | 0.1358 | 0.02789
Nitrógeno | 0.1408 | 0.03913
Dióxido de nitrógeno | 0.5354 | 0.04424
Óxido nitroso | 0.3832 | 0.04415
Oxígeno | 0.1378 | 0.03183
Pentano | 1.926 | 0.146
Fosfina | 0.4692 | 0.05156
Propano | 0.8779 | 0.08445
Silano | 0.4377 | 0.05786
Tetrafluoruro de silicio | 0.4251 | 0.05571
Dióxido de azufre | 0.6803 | 0.05636
Cloruro de estaño | 2.727 | 0.1642
Tolueno | 2.438 | 0.1463
Agua | 0.5536 | 0.03049
Xenón | 0.4250 | 0.05105
ID:(9648, 0)
Representación gráfica ecuación de Van der Waals
Ejercicio 
La ecuación de Van der Waals presenta un área de menores temperaturas en que existe una situación en que\\n\\n
$\displaystyle\frac{\partial p}{\partial V}\geq 0$
que representa un estado inestable. La pregunta es como se comporta el sistema en esta sección de la curva para lo que se debe recordar que en todo momento la energía de Gibbs debe ser un mínimo con :
| $ \Delta G_0 =\mbox{minimo}$ |
Por ello debemos representar la energía de Gibbs
ID:(864, 0)
Aplicación a Gas de Van der Waals
Descripción 
La ecuación de estado de Van der Waals tiene la peculiaridad de describir estados que no son estables. Un análisis mas detallado muestran que representan la fase liquida del sistema. Su estudio muestra como se puede emplear la energía libre de Gibbs para entender un sistema de dos fases.\\n\\nComo referencia se puede consultar el articulo Thermodynamic Properties of the van der Waals Fluid de David C. Johnston.
Variables
Cálculos
Cálculos
Ecuaciones
Ejemplos
Dado que el m nimo de la energ a de Gibbs requiere de que la compresibilidad sea positiva con
| $\left(\displaystyle\frac{\partial^2 G_0}{\partial V^2}\right)_T=-\left(\displaystyle\frac{\partial\bar{p}}{\partial V}\right)_T$ |
se concluye que al ser con
| $ k_p =-\displaystyle\frac{ DV_{p,T} }{ V }$ |
\\n\\nla ecuaci n de Van der Waals muestra una inestable en la secci n en que\\n\\n
$\displaystyle\frac{\partial p}{\partial V}> 0$
La regi n inestable separa una regi n de gran volumen molar y de alta compresibilidad, como en un gas, de una regi n de bajo volumen molar y baja compresibilidad, como en un liquido. Por ello se visualiza que la ecuaci n de Van der Waals podr a representar un gas pero tambi n, en condiciones apropiadas, un liquido. El sector de inestabilidad estar a relacionado con el cambio de fase.
(ID 9044)
Para comprender como se comporta el sistema en la zona en que la pendiente presi n volumen es positiva debemos estudiar la curva volumen temperatura entre las presi n
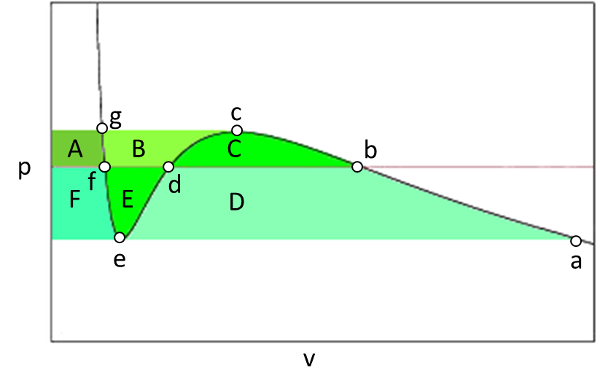
\\n\\nFunci n de Gibbs para el gas de Van Der Waals\\n\\nEn esta gr fica podemos ir calculando las energ as de Gibbs que se van dando en los distintos puntos a hasta g de la curva. As tenemos que inicialmente la energ a de Gibbs crece del punto a, al b y al c:\\n\\n
$g_b = g_a + D + E + F$
\\n\\n
$g_c = g_b + A + B + C = g_a + D + E + F + A + B + C$
\\n\\nA partir del punto c va decreciendo hasta el punto d y luego e\\n\\n
$g_d = g_b - A - B = g_a + D + E + F + C$
\\n\\n
$g_e = g_d - E - F = g_a + D + C$
\\n\\nFinalmente vuelve a crecer hasta el punto f y luego g\\n\\n
$g_f = g_e + F = g_a + D + C + F$
\\n\\n
$g_g = g_f + A = g_a + D + C + F + A$
(ID 1979)
Si se grafican los puntos a hasta f notaremos que la funci n tiene tres segmentos:
• inicial creciente entre a y c hasta un m ximo de $g_c = g_a + A + B + C + D + E + F$
• decreciente entre c y e hasta un valor de $g_e = g_a + C + D < g_c$
• nuevamente creciente entre e y g hasta un valor de $g_g = g_a + A + F + C + D < g_c$
Al ser
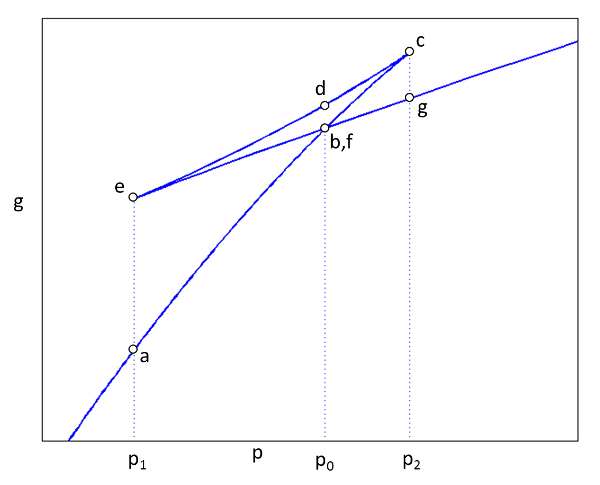
\\n\\nEn ese caso se tendr a que\\n\\n
$g_b = g_f$
lo que lleva a que las reas C y E deben ser iguales. Como el sistema en equilibro siempre tendr una energ a libre de Gibbs m nima, se concluye que el sistema tiene que permanecer en el punto de intersecci n o sea pasa directamente del punto b al punto f o viceversa.
(ID 1994)
Las siguientes constantes de la ecuaci n de Van der Waals:
En Sistema Internacional (SI)
Compuesto | a (J m3/mol2) | b (10-3 m3/mol)
----------------|:------------------:|:---------------------:
cido ac tico | 1.782 | 0.1068
Anh drido ac tico | 2.016 | 0.1263
Acetona | 1.409 | 0.0994
Acetonitrilo | 1.781 | 0.1168
Acetileno | 0.445 | 0.05136
Amon aco | 0.423 | 0.03707
Arg n | 0.136 | 0.03219
Benceno | 1.824 | 0.1154
Bromobenceno | 2.894 | 0.1539
Butano | 1.466 | 0.1226
Di xido de carbono | 0.364 | 0.04267
Sulfuro de carbono | 1.177 | 0.07685
Mon xido de carbono | 0.151 | 0.03985
Cloruro de carbono (IV) | 1.975 | 0.1281
Cloro | 0.658 | 0.05622
Clorobenceno | 2.577 | 0.1453
Cloroetano | 1.105 | 0.08651
Clorometano | 0.757 | 0.06483
Cian geno | 0.777 | 0.06901
Ciclohexano | 2.311 | 0.1424
ter diet lico | 1.761 | 0.1344
Sulfuro de dietilo | 1.900 | 0.1214
ter de dimetilo | 0.818 | 0.07246
Sulfuro de dimetilo | 1.304 | 0.09213
Etano | 0.556 | 0.0638
Etanotiol | 1.139 | 0.08098
Etanol | 1.218 | 0.08407
Acetato de etilo | 2.072 | 0.1412
Etilamina | 1.074 | 0.08409
Fluorobenceno | 2.019 | 0.1286
Fluorometano | 0.469 | 0.05264
Fre n | 1.078 | 0.0998
Tetracloruro de germanio | 2.290 | 0.1485
Helio | 0.0035 | 0.0237
Hexano | 2.471 | 0.1735
Hidr geno | 0.0248 | 0.02661
Bromuro de hidr geno | 0.4510 | 0.04431
Cloruro de hidr geno | 0.372 | 0.04081
Seleniuro de hidr geno | 0.534 | 0.04637
Sulfuro de hidr geno | 0.449 | 0.04287
Iodobenceno | 3.352 | 0.1656
Kript n | 0.235 | 0.03978
Mercurio | 0.820 | 0.01696
Metano | 0.228 | 0.04278
Metanol | 0.965 | 0.06702
Ne n | 0.0213 | 0.01709
xido n trico | 0.1358 | 0.02789
Nitr geno | 0.1408 | 0.03913
Di xido de nitr geno | 0.5354 | 0.04424
xido nitroso | 0.3832 | 0.04415
Ox geno | 0.1378 | 0.03183
Pentano | 1.926 | 0.146
Fosfina | 0.4692 | 0.05156
Propano | 0.8779 | 0.08445
Silano | 0.4377 | 0.05786
Tetrafluoruro de silicio | 0.4251 | 0.05571
Di xido de azufre | 0.6803 | 0.05636
Cloruro de esta o | 2.727 | 0.1642
Tolueno | 2.438 | 0.1463
Agua | 0.5536 | 0.03049
Xen n | 0.4250 | 0.05105
(ID 9648)
La ecuaci n de Van der Waals presenta un rea de menores temperaturas en que existe una situaci n en que\\n\\n
$\displaystyle\frac{\partial p}{\partial V}\geq 0$
que representa un estado inestable. La pregunta es como se comporta el sistema en esta secci n de la curva para lo que se debe recordar que en todo momento la energ a de Gibbs debe ser un m nimo con :
| $ \Delta G_0 =\mbox{minimo}$ |
Por ello debemos representar la energ a de Gibbs
(ID 864)
ID:(556, 0)
