Échange de particules
Storyboard 
L'échange de substances entre l'atmosphère et l'océan peut inclure des particules. Ceci est particulièrement pertinent lors de l'étude du transfert de molécules de CO2 de l'atmosphère vers l'océan.
Ocean-Atmosphere Interactions of Gases and Particles, Peter S. Liss, Martin T. Johnson (eds.). Springer, 2014
Chapter: Transfer Across the Air-Sea Interface
ID:(1630, 0)
Diffusion de CO2
Image 
Le CO2 est absorbé par les océans, ce qui contribue à atténuer son effet sur l'atmosphère et à retarder le changement climatique. Cependant, les processus impliqués sont plus complexes et comprennent :
- Échange gazeux avec l\'atmosphère : L\'océan et l\'atmosphère sont en constante échange de CO2 par diffusion des gaz. Le CO2 atmosphérique se dissout à la surface de l\'océan et forme de l\'acide carbonique (H2CO3), qui se dissocie ensuite en ions hydrogène (H+) et en bicarbonate (HCO3-). Ce processus aide à équilibrer les niveaux de CO2 entre l\'océan et l\'atmosphère.
- Photosynthèse et respiration : Les organismes marins tels que le phytoplancton et les algues réalisent la photosynthèse et absorbent le CO2 de l\'eau pour produire de la matière organique et libérer de l\'oxygène. Ce processus, appelé fixation du carbone, contribue à extraire le CO2 de l\'océan. Cependant, les organismes marins respirent également, ce qui signifie qu\'ils libèrent du CO2 dans l\'eau lors de la décomposition de la matière organique.
- Circulation océanique : L\'océan est caractérisé par sa circulation mondiale, au cours de laquelle les courants transportent de l\'eau riche en CO2 de la surface vers les profondeurs et vice versa. Cela contribue à la distribution et au mélange du CO2 dans l\'ensemble de l\'océan, permettant aux eaux profondes de stocker d\'importantes quantités de CO2 dissous.
- Sédimentation et enfouissement : Une partie de la matière organique produite par les organismes marins, y compris le CO2 capturé par la photosynthèse, peut s\'enfoncer et être enfouie au fond de l\'océan. Au fil du temps géologique, les sédiments s\'accumulent et le carbone organique est enfoui, pouvant être stocké dans le fond marin pendant de très longues périodes.
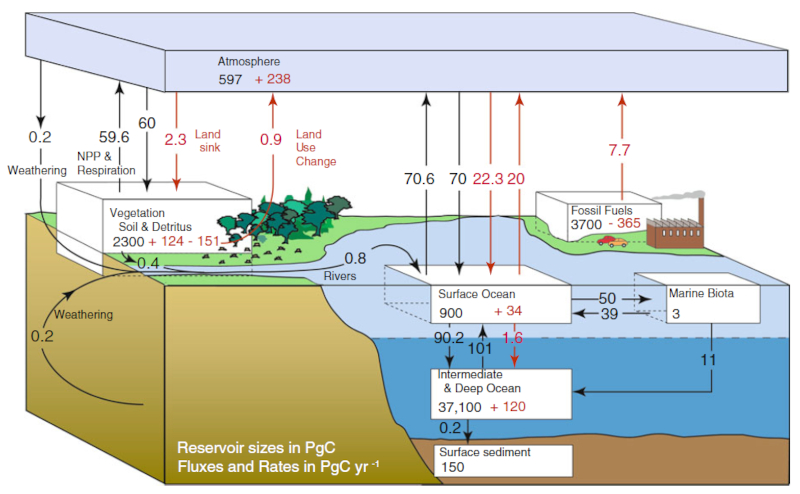
Flux de carbone annuel en PgC/an. Les chiffres en noir représentent la révolution préindustrielle, en rouge les augmentations liées à la révolution industrielle. Ocean-Atmosphere Interactions of Gases and Particles, Peter S. Liss Martin T. Johnson (Editors), Springer, 2014
Selon la zone et l'époque de la planète, il y a une plus grande concentration de carbone dans l'atmosphère que dans l'océan ou vice versa, définissant ainsi si le flux de carbone se fait de l'air vers l'eau ou vice versa.
ID:(12297, 0)
Vitesse de transfert et vitesse relative
Noter 
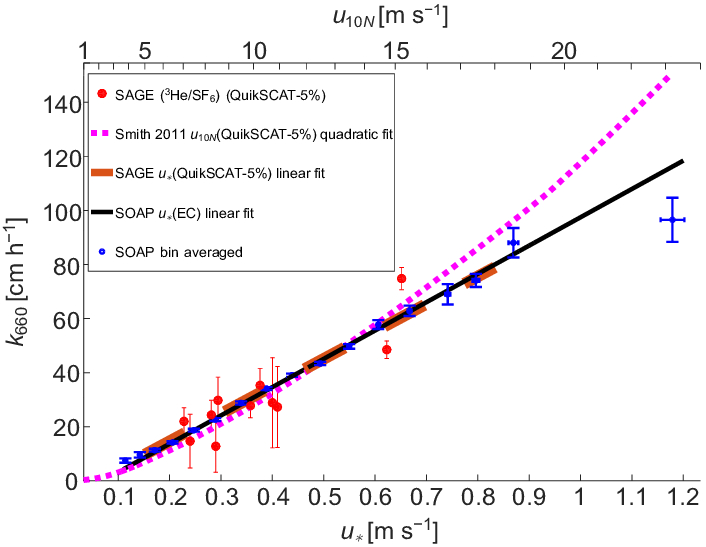
Dans une première approximation, la dépendance de a taux de transfert de gaz dans l'eau ($k_w$) par rapport à la vitesse relative, calculée en soustrayant ERROR:9437 de ERROR:9408, est proportionnelle à
$k_w \propto u_a - u_w$
comme observé dans le graphique :
ID:(12298, 0)
Vitesse de transfert et nombre de Schmidt
Citation 
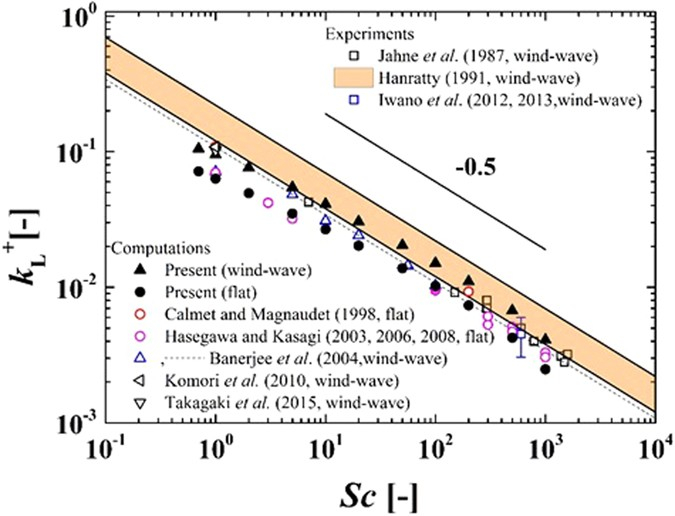
La relation entre a taux de transfert de gaz dans l'eau ($k_w$) est inversement proportionnelle à Le numéro de Schmidt ($Sc$), donc elle est exprimée comme étant proportionnelle à ce nombre élevé à ERROR:9926, qui est négatif :
$k_w\propto Sc^n$
ceci est représenté avec ERROR:9926 égal à -0.5 :
ID:(12299, 0)
Solubilité en fonction du nombre de Schmidt
Exercer 
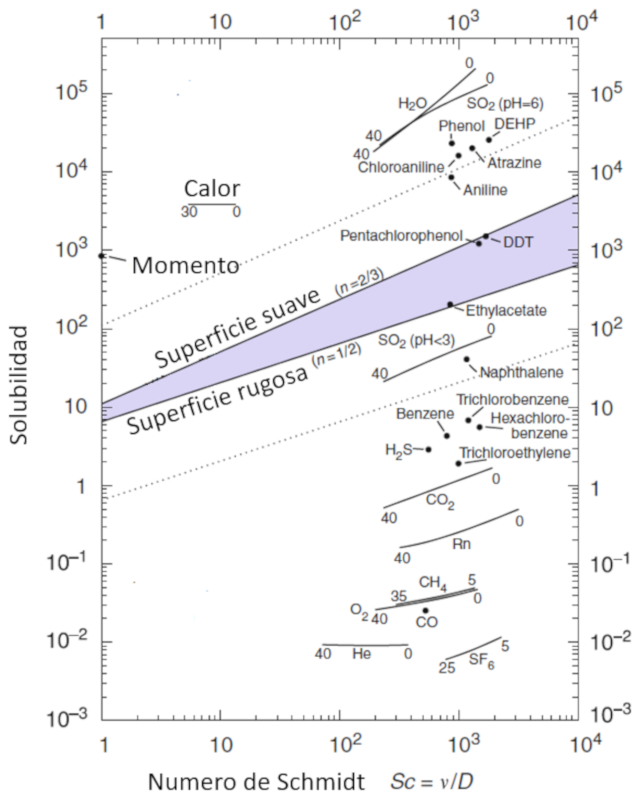
La mobilité des molécules, représentée par a solubilité du gaz ($\alpha$), est une fonction de la concentration de particules, décrite par le numéro de Schmidt ($Sc$), qui à son tour est calculée à partir de ERROR:9412, ERROR:9413 et ERROR:9414 selon l'équation suivante :
| $ Sc =\displaystyle\frac{ \eta }{ \rho D }$ |
Cette relation est illustrée dans le schéma suivant :
ID:(12245, 0)
Échange de CO2, vitesse de l'eau
Équation 
A taux de transfert de gaz dans l'eau ($k_w$) peut être modélisé en utilisant des données mesurées. Tout d'abord, il dépend de la vitesse à laquelle le système élimine le carbone de l'interface air-eau, ce qui rend la vitesse de transport proportionnelle à la vitesse relative entre les deux milieux.
Deuxièmement, il y a un effet de la mobilité des ions, qui peut être décrit par le numéro de Schmidt ($Sc$), représentant la relation entre la diffusion de l'impulsion et les particules. Cependant, cette dépendance n'est pas linéaire et est influencée par un facteur ERROR:9926 qui varie entre -1/2 et -2/3 en fonction de la rugosité de la surface.
Enfin, a taux de transfert de gaz dans l'eau ($k_w$) dépend également de ERROR:9409, qui est à son tour déterminé par le niveau de rugosité de la surface.
En résumé, le gaz a taux de transfert de gaz dans l'eau ($k_w$) est décrit en fonction de ERROR:9437, ERROR:9408, le numéro de Schmidt ($Sc$), ERROR:9409 et ERROR:9926 de la manière suivante :
| $ k_w = ( u_a - u_w ) \beta Sc ^ n $ |
ID:(15652, 0)
Échange de particules
Storyboard 
L'échange de substances entre l'atmosphère et l'océan peut inclure des particules. Ceci est particulièrement pertinent lors de l'étude du transfert de molécules de CO2 de l'atmosphère vers l'océan. Ocean-Atmosphere Interactions of Gases and Particles, Peter S. Liss, Martin T. Johnson (eds.). Springer, 2014 Chapter: Transfer Across the Air-Sea Interface
Variables
Calculs
Calculs
Équations
Si nous consid rons le flux de gaz $F$ et la vitesse de transport $k$, selon la relation g n rale :
En rempla ant la diff rence de concentration $C_0 - C_b$ par la diff rence de pression partielle du gaz en utilisant la solubilit $\alpha$, nous obtenons :
$C_0 - C_b = \alpha \Delta p_{CO2}$
nous pouvons alors obtenir :
Dans le mod le de similarit de Monin-Obukhov (MOST), le flux d' l ments tels que les gaz est estim en tenant compte de la diff rence de concentrations entre l'air et l\'eau, repr sent e par
$C_z - C_0$
et le flux est calcul en utilisant le coefficient de transfert $D_C$ et la vitesse de surface $U_z$, de la mani re suivante :
Cela permet d\'estimer le flux des l ments entre l\'air et l\'eau.
Le flux diffusif $F$ est d crit par la loi de Fick :
o $D$ est la constante de diffusion et $dC/dx$ est le gradient de concentration. En d finissant une vitesse de transfert comme suit :
nous pouvons tablir une quation de flux de la forme :
Exemples
Le CO2 est absorb par les oc ans, ce qui contribue att nuer son effet sur l'atmosph re et retarder le changement climatique. Cependant, les processus impliqu s sont plus complexes et comprennent :
- change gazeux avec l\'atmosph re : L\'oc an et l\'atmosph re sont en constante change de CO2 par diffusion des gaz. Le CO2 atmosph rique se dissout la surface de l\'oc an et forme de l\'acide carbonique (H2CO3), qui se dissocie ensuite en ions hydrog ne (H+) et en bicarbonate (HCO3-). Ce processus aide quilibrer les niveaux de CO2 entre l\'oc an et l\'atmosph re.
- Photosynth se et respiration : Les organismes marins tels que le phytoplancton et les algues r alisent la photosynth se et absorbent le CO2 de l\'eau pour produire de la mati re organique et lib rer de l\'oxyg ne. Ce processus, appel fixation du carbone, contribue extraire le CO2 de l\'oc an. Cependant, les organismes marins respirent galement, ce qui signifie qu\'ils lib rent du CO2 dans l\'eau lors de la d composition de la mati re organique.
- Circulation oc anique : L\'oc an est caract ris par sa circulation mondiale, au cours de laquelle les courants transportent de l\'eau riche en CO2 de la surface vers les profondeurs et vice versa. Cela contribue la distribution et au m lange du CO2 dans l\'ensemble de l\'oc an, permettant aux eaux profondes de stocker d\'importantes quantit s de CO2 dissous.
- S dimentation et enfouissement : Une partie de la mati re organique produite par les organismes marins, y compris le CO2 captur par la photosynth se, peut s\'enfoncer et tre enfouie au fond de l\'oc an. Au fil du temps g ologique, les s diments s\'accumulent et le carbone organique est enfoui, pouvant tre stock dans le fond marin pendant de tr s longues p riodes.
Selon la zone et l' poque de la plan te, il y a une plus grande concentration de carbone dans l'atmosph re que dans l'oc an ou vice versa, d finissant ainsi si le flux de carbone se fait de l'air vers l'eau ou vice versa.
Dans une premi re approximation, la d pendance de a taux de transfert de gaz dans l'eau ($k_w$) par rapport la vitesse relative, calcul e en soustrayant ERROR:9437 de ERROR:9408, est proportionnelle
$k_w \propto u_a - u_w$
comme observ dans le graphique :
La relation entre a taux de transfert de gaz dans l'eau ($k_w$) est inversement proportionnelle le numéro de Schmidt ($Sc$), donc elle est exprim e comme tant proportionnelle ce nombre lev ERROR:9926, qui est n gatif :
$k_w\propto Sc^n$
ceci est repr sent avec ERROR:9926 gal -0.5 :
La mobilit des mol cules, repr sent e par a solubilité du gaz ($\alpha$), est une fonction de la concentration de particules, d crite par le numéro de Schmidt ($Sc$), qui son tour est calcul e partir de ERROR:9412, ERROR:9413 et ERROR:9414 selon l' quation suivante :
Cette relation est illustr e dans le sch ma suivant :
A taux de transfert de gaz dans l'eau ($k_w$) peut tre mod lis en utilisant des donn es mesur es. Tout d'abord, il d pend de la vitesse laquelle le syst me limine le carbone de l'interface air-eau, ce qui rend la vitesse de transport proportionnelle la vitesse relative entre les deux milieux.
Deuxi mement, il y a un effet de la mobilit des ions, qui peut tre d crit par le numéro de Schmidt ($Sc$), repr sentant la relation entre la diffusion de l'impulsion et les particules. Cependant, cette d pendance n'est pas lin aire et est influenc e par un facteur ERROR:9926 qui varie entre -1/2 et -2/3 en fonction de la rugosit de la surface.
Enfin, a taux de transfert de gaz dans l'eau ($k_w$) d pend galement de ERROR:9409, qui est son tour d termin par le niveau de rugosit de la surface.
En r sum , le gaz a taux de transfert de gaz dans l'eau ($k_w$) est d crit en fonction de ERROR:9437, ERROR:9408, le numéro de Schmidt ($Sc$), ERROR:9409 et ERROR:9926 de la mani re suivante :
tant donn que le fluxe diffusif $F$ peut tre mod lis l\'aide de la loi de Fick :
Nous pouvons tablir une relation entre la vitesse de transfert $k$ et la diff rence de concentration $\Delta C$ de la mani re suivante :
En utilisant le mod le de similarit de Monin-Obukhov (MOST), il est possible d'estimer le flux d' l ments tels que les gaz en tenant compte du d placement de la surface et d\'un coefficient de transfert, qui s\'exprime de la mani re suivante:
Le gradient de concentration entre a concentration de gaz dans l'atmosphère ($C_{a,0}$) et a concentration de gaz dans l'eau ($C_{w,0}$) d pend de a solubilité du gaz ($\alpha$). Par cons quent, la relation suivante est tablie :
La vitesse de transfert d\'une quantit $k$ est d finie comme le flux $F$ divis par la diff rence de concentration entre les deux milieux, repr sent e par
$C_0-C_b$
Par cons quent, elle peut tre exprim e comme suit:
A taux de transfert de gaz dans l'air ($k_a$) peut tre estim partir de la loi de Fick, en comparant ERROR:9414 avec ERROR:9430 de la mani re suivante :
La vitesse de transfert du CO2 de l\'atmosph re vers l\'eau peut tre mod lis e en utilisant une quation similaire la r gle g n rale
Dans ce mod le, la diff rence de concentration est remplac e par la diff rence de pression partielle du gaz et sa solubilit $\alpha$. L\' quation peut tre exprim e de la mani re suivante:
Le param tre du gaz a taux de transfert de gaz dans l'eau ($k_w$) est d crit en fonction de ERROR:9437, ERROR:9408, le numéro de Schmidt ($Sc$), ERROR:9409 et ERROR:9926 comme suit :
Si nous supposons qu'il y a une transition continue dans la densit d' nergie l'interface entre l'air et l'eau, et consid rons que cette nergie est de nature cin tique, alors avec a densité de l'air ($\rho_a$), ERROR:9408 et ERROR:9438, ERROR:9437, nous pouvons tablir la relation suivante :
$\rho_a u_a^2=\rho_w u_w^2$
Ainsi, nous pouvons tablir la relation :
De plus, nous pouvons consid rer que la densit d' nergie a la m me unit que la tension superficielle, ce qui explique l' galit en fonction du fait que dans un syst me en quilibre, les tensions doivent tre gales.
Le nombre de Schmidt tablit une relation entre la diffusion visqueuse
et la diffusion des particules
La diffusion visqueuse est gale la viscosit divis e par la densit , tandis que la diffusion des particules correspond la constante de diffusion. Par cons quent, il est d fini comme suit :
ID:(1630, 0)
